Denne artikkelen er produsert og finansiert av Sintef - les mer.

En bitte liten lever, et ørlite hjerte eller en tynntarm kan nå vokse på en mikrochip
Denne sammenkoblingen åpner for uante forskningsmuligheter.
– Med denne teknologien kan vi studere og etterlikne fosterstadiet, en menstruasjonssyklus eller studere hvordan kreft spres, for å nevne noe. Og ikke minst: Denne teknologien forventes å minimere andelen dyreforsøk.
Det forteller forsker Frøydis Sved Skottvoll i Sintef.
Det hele startet med japaneren Shinya Yamanaka. Da han lyktes med å reprogrammere en hudcelle til å bli en stamcelle, revolusjonerte han stamcelle-verden.
På denne måten ble stamceller plutselig allment tilgjengelig. Nyvinningen ga Yamanaka Nobelprisen i medisin i 2012.
Gror små miniorganer
Noen år senere klarte forskere å gro de første miniorganene med en stamcelle som utgangspunkt. Det er det som i dag kalles organoider.
Nå jobbes det med å utvikle teknologien – rettere sagt den delen av teknologien som handler om mikrosystemet som organoidene studeres i.
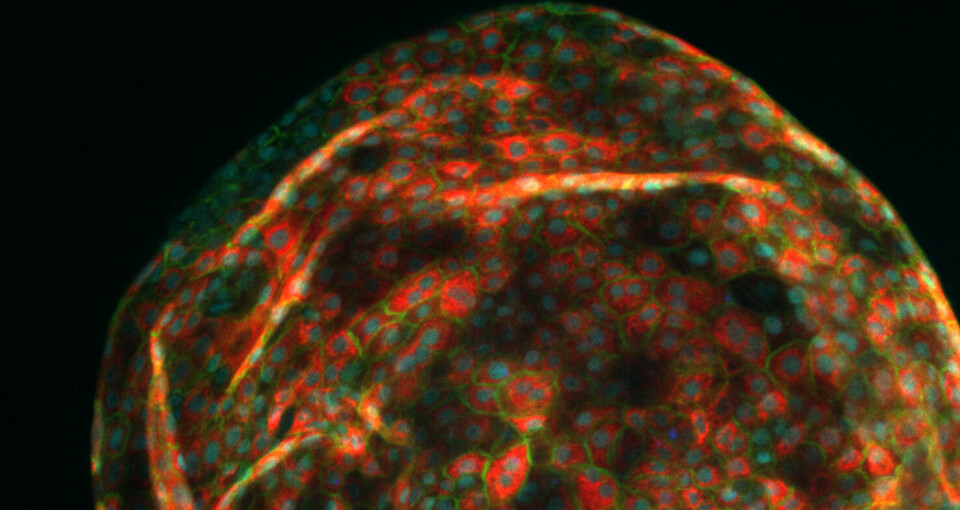
– Dette gjør vi ved å bruke fabrikasjonsmetoder fra databrikke-industrien til å utvikle skreddersydde mikrokanaler og sensorer som simulerer kroppens egne prosesser. I tillegg kan vi måle hvordan organoidene har det inne i mikrosystemet, forklarer forskeren.
Hva er egentlig «organ on a chip»?
Teknologien består av to elementer: et miniorgan, dyrket fram av en stamcelle, og en bitte liten og tredimensjonal brikke som består av ørsmå kanaler på hver sin side av en membran.
I disse kanalene kan forskerne tilsette ulike molekyler som gir cellene ulike signaler. Deretter kan de påvirke gjennomstrømningen av dem.
Membranen fungerer som en porøs skillevegg. Den gjør at molekyler kan transporteres mellom to ulike mini-organer, litt som blodåreveggen.
Målet er å simulere den biologiske aktiviteten som skjer på cellenivå i kroppen.

Skottvoll forteller at teknologien også kan brukes til å simulere for eksempel det som kalles blod-hjerne-barrieren. Dette er kroppens sikkerhetsmekanisme for å beskytte slik at at det ikke lekker stoffer mellom hjernen og blodbanen.
– Hjernen ligger altså helt atskilt fra blodbanen. Det er i utgangspunktet bra, men det kan være en ulempe om vi vil inn i hjernen med for eksempel medisiner, utdyper hun.
Historisk sett har det vært veldig vanskelig å studere denne funksjonen i mennesker. Men med «organ on a chip» har dette blitt mulig.
En stamcelle kan bli til alt fra blodceller til muskelceller
I tillegg til å ha en mikrostruktur som kan etterlikne biologien i en celle, trengs det en stamcelle som «frø» for prosessen. Men hva er egentlig det?
Ifølge Bioteknologirådet er stamceller utgangspunktet for alle kroppens celler og vev. Men de er også ansvarlige for vedlikehold og reparasjoner av skadet vev.
Disse cellene har en unik evne til å fornye og dele seg over lang tid. De kan også danne mer spesialiserte celler gjennom en prosess hvor en stamcelle blir «mor» til alt fra blodceller til muskelceller. Men en stamcelle kan aldri bli til kjønnsceller.
– Om vi vet hva som skal til, er det litt som å stelle en surdeig: Den første dagen gjør du ett steg. Dag to tilsetter du noe annet. Deretter må man røre, vente og etter hvert tilsette flere ingredienser. Slik kan vi fortsette til vi ser at cellene har blitt til et miniorgan. Noen ganger likner de til og med på et faktisk organ i fasongen, forteller Skottvoll.
Organoider kan gi oss mange svar
Forskeren var tidlig ute med å fange interesse for teknologien. Allerede som doktorgradsstipendiat ved Universitetet i Oslo begynte hun å jobbe med «organ-on-a-chip».
Det Skottvoll så på, var rett og slett hvor mye en mini-lever likner på en ekte lever når den ble utsatt for ulike legemidler.
– Det jeg fant, var at de er veldig like en menneskelever.
Men at de er litt «tregere» enn et ekte organ når det gjelder å bryte ned medisinene. I praksis betyr det at forsøk på slike organer kan ta tid, fordi mini-organet ikke er «helt ferdig».
– Vi tror at årsaken til dette er at organene enda ikke har utviklet blodårer. Det er altså ikke et system som kan frakte medisiner rundt i organet, sier forskeren.
Kan simulere «alt»
Den fysiske forutsetningen for «organ-on-a-chip» er altså en mikroskopisk struktur som består av ulike kanaler og membraner. Og det er slike fysiske mikrostrukturer som nå blir til i Sintef MinaLab i Gaustadbekkdalen i Oslo.
– Like viktig som å lage organ-on-a-chip, er det å måle hva som egentlig skjer. Derfor utvikler vi også sensorteknologi. Den kan automatisk overvåke og måle hvordan mini-organene har det på chipen, sier Skottvoll.
Farvel til dyreforsøk, og raskere utvikling av medisiner?
I framtida kan det altså hende at dyreforsøk blir unødvendig. Vi kan dyrke fram organer i stedet for å bruke organdonorer. Videre kan vi teste ut behandlingsmetoder og medisiner på «ekte» organer.
I dag er det faktisk mulig å stimulere celler på så avanserte måter at vi kan simulere for eksempel fosterutviklingen i en cellekultur i et laboratorium.
– Dette er naturligvis en arena som åpner for en rekke etiske diskusjoner om hva som er forskningsetisk riktig. Særlig debatten om hjerneorganoider er et hot tema om dagen, sier Skottvoll.
Mer persontilpasset medisin
Men det er ikke tvil om at dette er en teknologi som kan brukes til å gi oss mer effektive behandlingsmetoder. Ikke minst innenfor det som kalles persontilpasset medisin.
Ifølge forskeren kommer dette til å endre måten vi velger riktig behandling til pasienter på.
Hun forteller at hvis pasienten har kreft i leveren, går det an å gro en pasientspesifikk mini-lever og bruke organ-on-a-chip til å simulere hvordan ulike behandlinger og medisiner påvirker kreften og pasientens lever.
– På denne måten kan vi unngå at behandlinger ikke fungerer eller personspesifikke bivirkninger fra medisiner, sier Frøydis Sved Skottvoll.
Les også disse artiklene fra Sintef:
-
Fikk nye vernesko – kunne droppe smertestillende
-
Nytt superstoff baner vei for oljefri skipsfart
-
– Vi kan skape nye stoffer av klærne du kaster
-
Når gjerder ikke er nok: Hvordan unngå å kollidere med dyr?
-
Slik kan elektriske skip lade i åpen sjø
-
Enormt basseng i Trondheim: Aldri er det stilt så høye krav til betong
































