Denne artikkelen er produsert og finansiert av Universitetet i Oslo - les mer.

Forskerne skrudde av gen for farger og skapte en albinotorsk
Dette forsøket med CRISPR-metoden er trolig første gang torsk er blitt genredigert.
– Da vi skulle teste metoden, valgte vi å gjøre det på et gen som er nødvendig for pigmentering, for det er enkelt å se, forklarer professor i biologi Finn-Eirik Johansen.
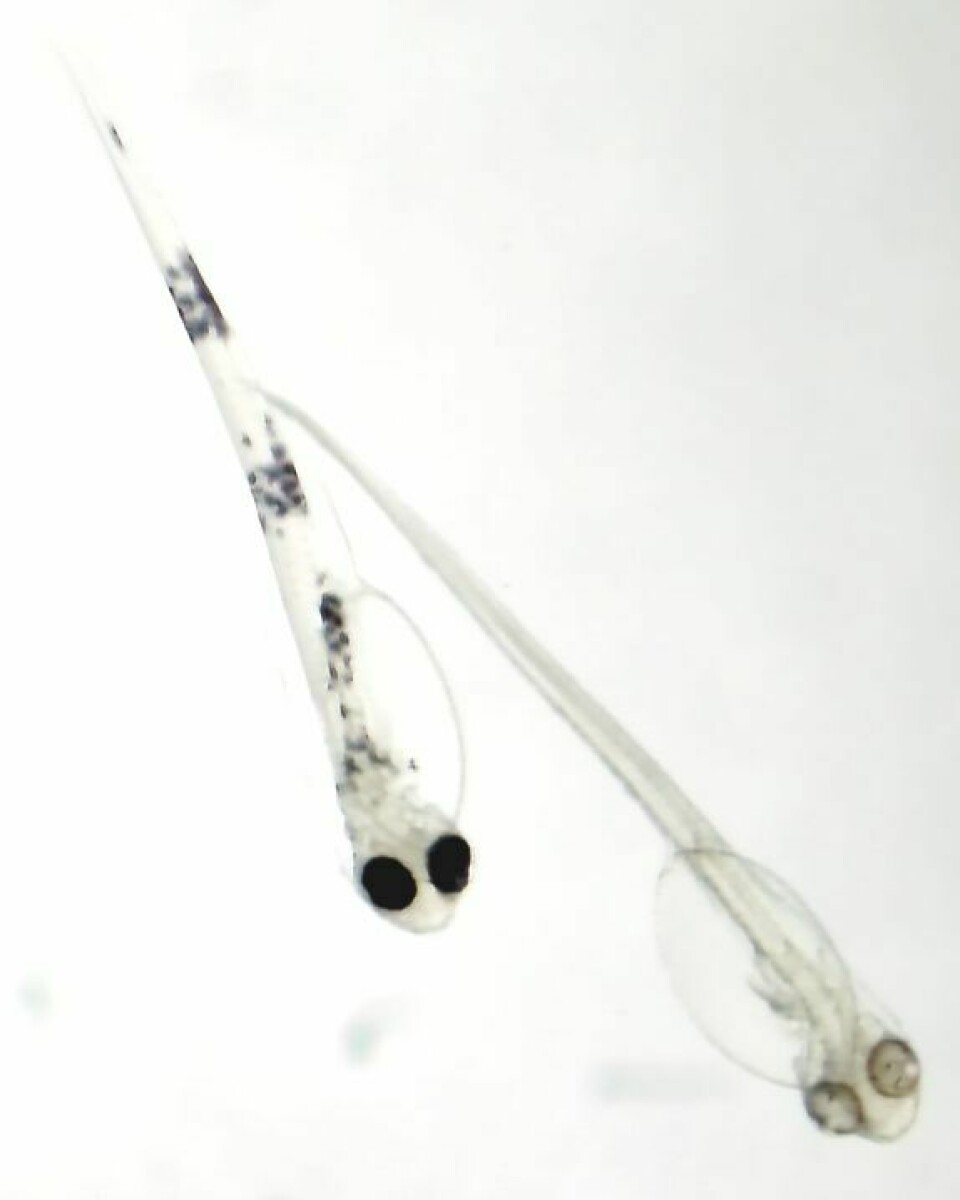
Han forklarer at forskerne har laget en metode for å bruke CRISPR til å genredigere torsk. For å vise at det er mulig, skrudde de av et gen for pigment, eller farger.
På den måten fikk de helt fargeløs torsk – albinotorsk. En slik mutasjon kan også oppstå i naturen, men det er svært sjelden.
Den første laksen som ble genredigert med CRISPR-metoden, kom allerede i 2014, men dette er trolig første gang det er gjort på torsk, forklarer han.
Selv om CRISPR-metoden kan brukes til mange ulike arter, så må den tilpasses for hver art.
Forskerne ved Institutt for biovitenskap ved Universitetet i Oslo har tilpasset metoden til bruk i torsk. Det dannes et skall rundt et befruktet torskeegg, derfor har det vært vanskelig å genredigere torsk.

Neste steg er å «slå av» deler av torskens immunforsvar
Johansen og de andre forskerne har samarbeidet med Nofima om prosjektet.
– Nofima ønsker en metode for å bruke CRISPR på torsk, og vi trengte tilgang til befruktede egg, forklarer Johansen.
Han forteller at Nofima tidligere har forsøkt å utvikle CRISPR-metoder for torsk, uten å lykkes.
– Noe av grunnen er at det er vanskelig å sprøyte inn det vi kaller gensaksen i egget, forklarer stipendiaten Adrián López-Porras, som har gjort tilpasningsarbeidet for å få metoden til å passe til torsk.

Torsken gyter bare i en kort sesong, så tilgang på egg og melke er begrenset. I tillegg er effektiviteten til befruktningen lav, selv om antall egg og spermier er høyt.
– Torskens strategi er store tall, forklarer Johansen.
Derfor er overlevelsesgraden til eggene også noe lavere. Etter befruktning dekkes torskeegget av et beskyttende skall. Dersom dette brytes, dør embryoet inni. Forskerne forklarer at dette er noe av årsaken til at det er vanskelig å få CRISPR-saksen inn i egget, for den må føres inn med en tynn glassprøyte.
På grunn av det korte tidsvinduet med tilgang til befruktede egg måtte forskerne teste mange ulike metoder samtidig. Dette førte til at Porras måtte sprøyte inn gensaksen i 8000 torskeegg på to uker for å finne en metode som kunne fungere.
Gleden var stor da eggene klekket og de kunne konstatere at de fikk hvit torskeyngel.
Målet er å forstå torskens immunforsvar
Johansen forteller at det er kommersiell interesse for å bruke CRISPR-metoden på torsk, men at deres motivasjon er en annen.
– Vi ønsker å forstå mer om torskens immunforsvar. Det har lenge vært kjent at T-cellene hjelper B-cellene å lage antistoffer i pattedyr. Men vi vet ikke om T- og B-celler samarbeider i torsk. Derfor ønsker vi blant annet å slå av T-cellene i torsk, forklarer han.
Ifølge Johansen kan bedre forståelse av torskens immunforsvar være viktig for oppdrettsnæringen. I tillegg vil det gi kunnskap om immunforsvarets evolusjon. Torsken viser seg å ha et immunforsvar som fungerer ganske annerledes enn hos pattedyr. Derfor er det spesielt interessant for forskerne å forstå.
Referanse:
Adrián López-Porras mfl.: CRISPR-Cas9/Cas12a-based genome editing in Atlantic cod (Gadus morhua). Aquaculture, 2024
Les også disse sakene fra Universitetet i Oslo:
-
Forskeren lærte å rydde miner i Kosovo. Få uker senere døde kurslederen
-
Forskere vil kartlegge romskrot med radar
-
– Den digitale forvaltningen av identitet i Norge er en katastrofe
-
Dette dobler sjansen for å droppe ut av skolen
-
Kvinne frisk av alvorlig autoimmun sykdom: – Kan endre måten vi behandler slike sykdommer på
-
– Det står ikke bra til med leseferdighetene i norsk skole
forskning.no vil gjerne høre fra deg!
Har du en tilbakemelding, spørsmål, ros eller kritikk? TA KONTAKT HER
































